7月,中美華東喜訊不斷:他克莫司膠囊獲首家過(guò)評(píng),2.2類新藥GRCE2101獲批臨床,2.1類新藥HDM3010首次申報(bào)臨床,公司的創(chuàng)新研發(fā)實(shí)力不斷提升。2020年以來(lái),公司在拳頭領(lǐng)域糖尿病用藥市場(chǎng)拿下了多個(gè)首仿,并成功撬開(kāi)了全身用抗真菌藥、內(nèi)分泌治療用藥兩大亞類市場(chǎng)的大門,首款生物類似藥利拉魯肽注射液在今年順利獲批,公司迎來(lái)了百花齊放的新局面。
11款新品火速上市,百億市場(chǎng)實(shí)現(xiàn)“零的突破”
杭州中美華東制藥是華東醫(yī)藥旗下一家綜合性制藥企業(yè),公司產(chǎn)品覆蓋移植免疫、內(nèi)分泌、慢性腎病、消化系統(tǒng)、抗生素、抗腫瘤以及心血管七大治療領(lǐng)域。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2020年至今公司已有11款新品獲批上市,每年均有重磅產(chǎn)品入局搶食,公司的市場(chǎng)競(jìng)爭(zhēng)力不斷提升。
表1:中美華東2020年以來(lái)獲批的新品情況
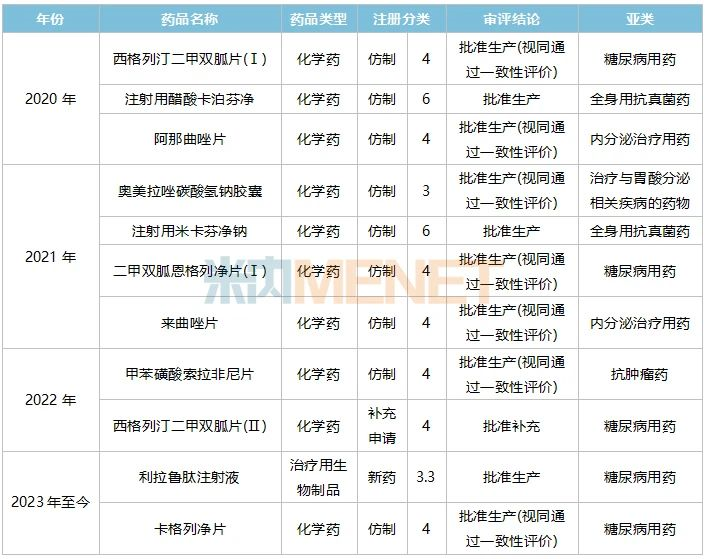
來(lái)源:米內(nèi)網(wǎng)中國(guó)申報(bào)進(jìn)度(MED)數(shù)據(jù)庫(kù)
糖尿病用藥是中美華東的拳頭領(lǐng)域之一,2020年公司拿下了西格列汀二甲雙胍片(Ⅰ),2021年拿下了二甲雙胍恩格列凈片(Ⅰ),2023年拿下了利拉魯肽注射液,3大產(chǎn)品均為國(guó)產(chǎn)首家,公司擁有先發(fā)優(yōu)勢(shì)。
西格列汀二甲雙胍片(Ⅰ)和二甲雙胍恩格列凈片(Ⅰ)為復(fù)方口服降糖藥,2020-2022年在中國(guó)城市公立醫(yī)院、縣級(jí)公立醫(yī)院、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡(jiǎn)稱中國(guó)公立醫(yī)療機(jī)構(gòu))終端,口服降糖藥復(fù)方的增長(zhǎng)率分別達(dá)到67.76%、78.21%、38.02%,銷售額在2022年漲至23億元以上,市場(chǎng)正進(jìn)入快速增長(zhǎng)階段。近幾年,多家國(guó)內(nèi)藥企加速布局,中美華東目前已有4款復(fù)方口服降糖藥獲批上市(按產(chǎn)品名統(tǒng)計(jì))。
圖1:中美華東已上市的復(fù)方口服降糖藥
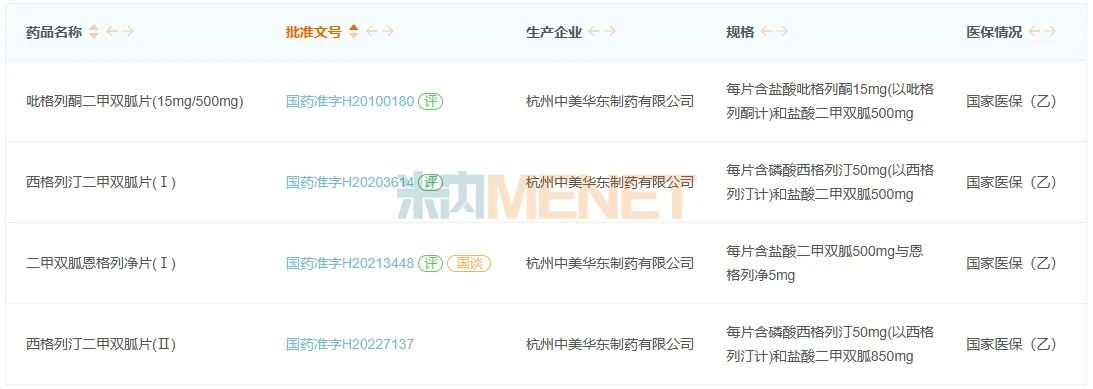
來(lái)源:米內(nèi)網(wǎng)中國(guó)上市藥品(MID)數(shù)據(jù)庫(kù)
利拉魯肽注射液是全球暢銷的GLP-1受體激動(dòng)劑之一,2022年原研產(chǎn)品減肥適應(yīng)癥的全球銷售額超過(guò)106億丹麥克朗(按即時(shí)匯率約15億美元),糖尿病適應(yīng)癥的全球銷售額超過(guò)123億丹麥克朗(按即時(shí)匯率約18億美元)。
利拉魯肽注射液是中美華東首個(gè)獲批上市的生物類似藥,2023年3月糖尿病適應(yīng)癥獲批,隨后在今年6月肥胖或超重適應(yīng)癥獲批,公司是國(guó)內(nèi)首家同時(shí)擁有利拉魯肽注射液糖尿病適應(yīng)癥及肥胖或超重適應(yīng)癥批文的藥企。華東醫(yī)藥在回復(fù)投資者提問(wèn)時(shí)表示,該產(chǎn)品正在全國(guó)各省開(kāi)展掛網(wǎng)和進(jìn)院工作,含肥胖與超重適應(yīng)癥的新包裝預(yù)計(jì)將于今年8月份上市銷售,該產(chǎn)品有望成為公司新的業(yè)績(jī)?cè)鲩L(zhǎng)點(diǎn)。
中美華東除了持續(xù)深耕糖尿病用藥市場(chǎng),還不斷擴(kuò)大其他領(lǐng)域的產(chǎn)品布局。2020年公司首款全身用抗真菌藥注射用醋酸卡泊芬凈獲批,正式入局這個(gè)火熱市場(chǎng)。2022年在中國(guó)公立醫(yī)療機(jī)構(gòu)終端,中美華東的注射用醋酸卡泊芬凈銷售額增長(zhǎng)率超過(guò)了349%,迎來(lái)了開(kāi)門紅。2021年公司第二款產(chǎn)品注射用米卡芬凈鈉順利上市,進(jìn)一步提升公司在全身用抗真菌藥市場(chǎng)的競(jìng)爭(zhēng)力。
2020年中美華東首款內(nèi)分泌治療用藥阿那曲唑片獲批上市,公司正式入局這個(gè)百億市場(chǎng)。2021年在中國(guó)公立醫(yī)療機(jī)構(gòu)終端,中美華東的阿那曲唑片銷售額增長(zhǎng)率超過(guò)2425%,2022年繼續(xù)保持正增長(zhǎng)。2021年公司在內(nèi)分泌治療用藥市場(chǎng)再添新品,來(lái)曲唑片順利上市。
19個(gè)產(chǎn)品已過(guò)評(píng),國(guó)采中標(biāo)產(chǎn)品份額飛升
中美華東首個(gè)過(guò)評(píng)產(chǎn)品阿卡波糖片在2018年11月獲批,2023年7月25日他克莫司膠囊首家過(guò)評(píng),截至目前公司已過(guò)評(píng)(含視同過(guò)評(píng))的產(chǎn)品數(shù)量達(dá)到19個(gè)。
表2:中美華東已過(guò)評(píng)/視同過(guò)評(píng)的產(chǎn)品情況
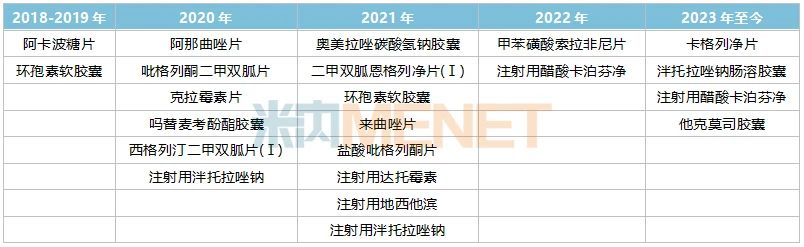
來(lái)源:米內(nèi)網(wǎng)中國(guó)申報(bào)進(jìn)度(MED)數(shù)據(jù)庫(kù)
二甲雙胍恩格列凈片(Ⅰ)、環(huán)孢素軟膠囊、西格列汀二甲雙胍片(Ⅰ)、阿卡波糖片以及他克莫司膠囊為首家過(guò)評(píng),泮托拉唑鈉腸溶膠囊、注射用醋酸卡泊芬凈、注射用達(dá)托霉素、鹽酸吡格列酮片、奧美拉唑碳酸氫鈉膠囊、來(lái)曲唑片、嗎替麥考酚酯膠囊、吡格列酮二甲雙胍片等為第二或第三家過(guò)評(píng),中美華東前三家過(guò)評(píng)率在68%以上。
表3:中美華東中標(biāo)國(guó)采的產(chǎn)品市場(chǎng)份額變化情況
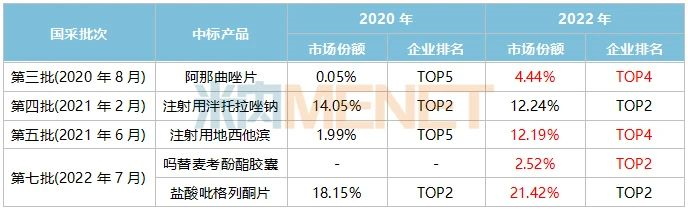
來(lái)源:米內(nèi)網(wǎng)中國(guó)公立醫(yī)療機(jī)構(gòu)藥品終端競(jìng)爭(zhēng)格局
中美華東積極參與國(guó)家集中帶量采購(gòu),從第三批國(guó)采開(kāi)始,第四批、第五批、第七批合計(jì)有5個(gè)產(chǎn)品順利中標(biāo)。阿那曲唑片、注射用地西他濱、嗎替麥考酚酯膠囊和鹽酸吡格列酮片2022年在中國(guó)公立醫(yī)療機(jī)構(gòu)終端的市場(chǎng)份額均有較大的提升。
公司已過(guò)評(píng)且暫未納入國(guó)采的產(chǎn)品中,注射用醋酸卡泊芬凈和奧美拉唑碳酸氫鈉膠囊目前的競(jìng)爭(zhēng)格局≥5家,或?qū)⒊蔀榈诰排鷩?guó)采的熱門產(chǎn)品。其中,注射用醋酸卡泊芬凈2022年在中國(guó)公立醫(yī)療機(jī)構(gòu)終端銷售額超過(guò)23億元,默沙東市場(chǎng)份額超過(guò)60%,中美華東的6類仿制上市申請(qǐng)于2020年獲批并于2022年通過(guò)一致性評(píng)價(jià),目前的市場(chǎng)份額不到1%,若該產(chǎn)品順利納入國(guó)采并中標(biāo),中美華東有望借助國(guó)采之力,實(shí)現(xiàn)“光腳品種”大爆發(fā)。
4款1類新藥全速推進(jìn),50億品種新劑型首仿來(lái)了
近幾年中美華東不斷加大研發(fā)投入,奮斗目標(biāo)是成為一家以科研開(kāi)發(fā)與技術(shù)創(chuàng)新為主導(dǎo)的創(chuàng)新型國(guó)際化醫(yī)藥工業(yè)企業(yè)。今年以來(lái),公司再有1款1類新藥和1款改良新藥獲批臨床,近日提交了HDM3010的臨床申請(qǐng),公司的新藥矩陣猛將如云。
表4:中美華東2023年至今申報(bào)的新藥情況
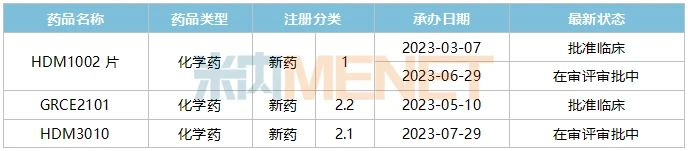
注:統(tǒng)計(jì)不含已上市產(chǎn)品新增適應(yīng)癥或功能主治
來(lái)源:米內(nèi)網(wǎng)中國(guó)申報(bào)進(jìn)度(MED)數(shù)據(jù)庫(kù)
HDM1002片是中美華東自主研發(fā)并擁有全球知識(shí)產(chǎn)權(quán)的化藥1類新藥,是一款具有口服活性、強(qiáng)效、高選擇性的GLP-1受體小分子完全激動(dòng)劑。公司于2023年3月在中國(guó)首次提交臨床申請(qǐng),獲批適應(yīng)癥為用于治療成人2型糖尿病,6月提交的臨床申請(qǐng)正在審評(píng)審批中。據(jù)悉,HDM1002片為中美雙報(bào)產(chǎn)品,該產(chǎn)品在美國(guó)的IND申請(qǐng)已于2023年5月獲批。
近日,公司的化藥2.2類新藥GRCE2101獲批臨床,適應(yīng)癥為用于動(dòng)脈硬化引起的缺血性心血管病變、缺血性腦血管病變、靜脈血栓形成,也可用于血液透析時(shí)預(yù)防血栓形成。
表5:中美華東部分在研的重磅新藥情況
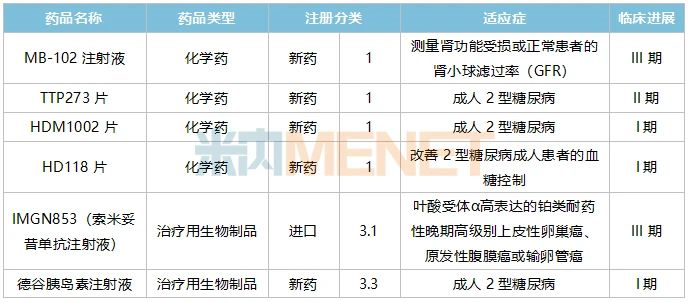
來(lái)源:米內(nèi)網(wǎng)中國(guó)臨床試驗(yàn)數(shù)據(jù)庫(kù)
目前進(jìn)展較快的1類新藥TTP273片、HDM1002片、HD118片均為糖尿病用藥,公司集中火力攻克這個(gè)百億市場(chǎng)。TTP273片是公司2017年從美國(guó)vTv公司引進(jìn)的口服GLP-1受體激動(dòng)劑小分子創(chuàng)新藥,目前II期臨床已完成。HD118片是公司于2014年從Sino-Med International公司引進(jìn)的DPP-4抑制劑,目前與公司自主研發(fā)的HDM1002片均在I期臨床階段。
公司首款生物類似藥利拉魯肽注射液的獲批,激勵(lì)著公司繼續(xù)加碼,早前已獲得了德谷胰島素注射液、地特胰島素注射液、門冬胰島素注射液的臨床批件,目前進(jìn)展最快的德谷胰島素注射液已在I期臨床階段。
7月12日華東醫(yī)藥發(fā)布公告稱,全資子公司中美華東與美國(guó)合作方ImmunoGen,Inc.合作開(kāi)發(fā)的索米妥昔單抗注射液(IMGN853)被納入優(yōu)先審評(píng)品種名單,根據(jù)合作協(xié)議,中美華東擁有該產(chǎn)品在大中華區(qū)(含中國(guó)大陸、香港、澳門和臺(tái)灣地區(qū))的獨(dú)家臨床開(kāi)發(fā)及商業(yè)化權(quán)益。公告中提到,索米妥昔單抗注射液被納入優(yōu)先審評(píng)后,公司計(jì)劃將于2023年第三季度正式向NMPA遞交附條件上市許可申請(qǐng)。
表6:中美華東報(bào)產(chǎn)在審的產(chǎn)品情況
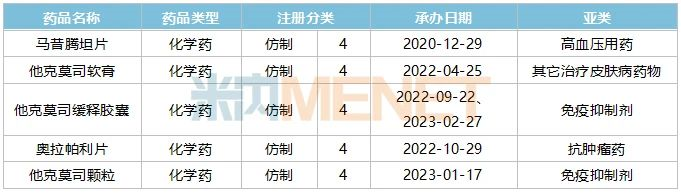
來(lái)源:米內(nèi)網(wǎng)中國(guó)申報(bào)進(jìn)度(MED)數(shù)據(jù)庫(kù)
仿制藥方面,中美華東有5款新品正在沖刺上市。馬昔騰坦片是一款抗肺動(dòng)脈高壓藥,原研產(chǎn)品2022年的全球銷售額超過(guò)17億美元,2017年獲批進(jìn)入國(guó)內(nèi)市場(chǎng)后在2019年進(jìn)入國(guó)家醫(yī)保談判目錄,2022年在中國(guó)公立醫(yī)療機(jī)構(gòu)終端的銷售額已漲至超過(guò)1.8億元。該產(chǎn)品目前暫未有國(guó)內(nèi)藥企獲得批文,中美華東依然有機(jī)會(huì)搶奪首仿。值得注意的是,公司在該亞類市場(chǎng)暫未有產(chǎn)品獲批上市,馬昔騰坦片有望成為公司首款獲批的高血壓用藥。
他克莫司是一種強(qiáng)力的新型免疫抑制劑,2022年在中國(guó)公立醫(yī)療機(jī)構(gòu)終端的銷售額已漲至58億元以上。中美華東在2008年拿下了他克莫司膠囊的生產(chǎn)批文,目前公司已成為該產(chǎn)品的國(guó)內(nèi)龍頭,2022年在中國(guó)公立醫(yī)療機(jī)構(gòu)終端的銷售額超過(guò)23億元。借助已有的市場(chǎng)優(yōu)勢(shì),中美華東提交了他克莫司軟膏、他克莫司緩釋膠囊、他克莫司顆粒的上市申請(qǐng),進(jìn)一步鞏固領(lǐng)軍地位,其中他克莫司顆粒目前暫未有國(guó)內(nèi)藥企獲得批文,中美華東是首家提交仿制上市的國(guó)內(nèi)藥企,搶首仿有時(shí)間優(yōu)勢(shì)。
資料來(lái)源:米內(nèi)網(wǎng)數(shù)據(jù)庫(kù)、公司公告等
注:米內(nèi)網(wǎng)《中國(guó)公立醫(yī)療機(jī)構(gòu)藥品終端競(jìng)爭(zhēng)格局》,統(tǒng)計(jì)范圍是:中國(guó)城市公立醫(yī)院、縣級(jí)公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院,不含民營(yíng)醫(yī)院、私人診所、村衛(wèi)生室;上述銷售額以產(chǎn)品在終端的平均零售價(jià)計(jì)算。數(shù)據(jù)統(tǒng)計(jì)截至8月1日,如有疏漏,歡迎指正!

